
让建站和SEO变得简单
让不懂建站的用户快速建站,让会建站的提高建站效率!

Science发布2025十大本事迫害, 中国龙东说念主、耐滚水稻皆上榜
企业文化
发布日期:2025-12-22 15:26 点击次数:118
2025 年,全球科研领域迎来了爆发式的迫害,科技不仅在实验室中刷新着领路的鸿沟,更在施行天下中回荡为重塑文雅的力量。当地时辰 12 月 18 日,知名学术期刊《科学》(Science)揭晓了其评比的 2025 年度十大科学迫害,这些本事朝上了能源出产、古东说念主类学、遗传工程及东说念主工智能等多个要道领域。本文将明白这十项本事,研究它们何如共同编织出东说念主类畴昔的新蓝图。
历史性拐点:绿色电力初度登顶

《科学》杂志将 2025 年度迫害授予可再生能源,因其初度杰出煤炭,成为全球最主要电力源流。这一历史性迁徙的中枢驱能源是中国的全面引颈。中国通过恒久产业政策,现已主导全球供应链,出产了约 80% 的太阳能电板、70% 的风力涡轮机和锂电板。
鸿沟化制造带来了成本鼎新,使惬心电力成为全球好多地区最低价的选拔,造成了降价刺激需求,需求扩大鸿沟的自我强化轮回。中国的能源转型鸿沟空前,其新增惬心装机容量相当于上百座核电站,并通过特高压电网将西部能源运输至东部城市。
同期,中国制造的清洁本事正改变天下,为巴基斯坦、南非等国度提供了低成本、高可靠的能源管束决策,推动了全球南边的能源自主。干系词,挑战依然存在:为均衡电网间歇性,中国仍在成立调峰煤电;全球贸易壁垒可能阻碍本事换取;万古储能和重工业脱碳等系统性难题待解。
但根人性转变断然发生,驱动能源鼎新的不再仅是征象包袱感,更是经济性与能源安全的刚性需求。这种市集内生能源的造成,确保了现时节点不是止境,而是通向无化石燃料畴昔的坚实早先,让全球碳排放达峰与深度减排的指标初度变得了了着实。
荒僻病治愈新纪元:首例个性化基因剪辑的得胜推行
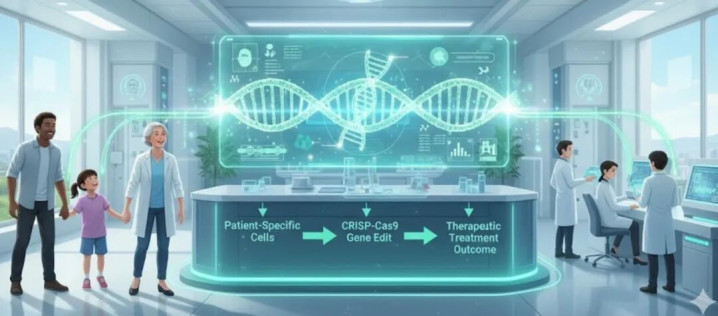
基因剪辑本事从普适性疗法迈向个性化精确医疗的里程碑于 2025 年收场。别称患有遗传性氨代谢很是疾病(CSP1 基因劣势)的男婴 KJ,成为全球首例接收定制化碱基剪辑治愈的患者。
传统率疗需严格罢休饮食或进行高风险肝移植,而新疗法通过预备针对其罕见基因突变的碱基剪辑器,应用脂质纳米颗粒寄递至肝脏。治愈后仅数月,KJ 的卵白质耐受材干进步,血氨水平得到限制,标记着针对超荒僻突变的基因剪辑从见识走向临床。
这一迫害的中枢在于监管与本事的协同创新。好意思国 FDA 首创性地允许将针对不同但类似基因劣势的微调疗法纳入兼并临床试验框架,极大简化了审批历程。这种平台化监管策略,为攻克因突变类型浩瀚而此前无法成药的数千种荒僻病提供了施行旅途,畴昔或可通过修改兼并剪辑器中枢模板,快速适配不同突变。
尽管远景纷乱,个性化基因剪辑仍濒临成本素雅、恒久安全性待考证等挑战。干系词,首例得胜案例已讲授:以 CRISPR 本事为基础,为单个患者量身定制基因疗法在本事上可行。这不仅为大宗佩戴罕见突变的荒僻病患者点火但愿,更预示着医疗范式向一东说念主一药的终极个性化期间迈进的要道一步。
完毕超等淋病危急:双再行药获批开启耐药菌反击战

在全球抗生素耐药性危急中,淋病——这一每年影响超 8000 万东说念主、可致不孕并加重艾滋病传播的疾病,因致病菌险些对扫数抗生素产生耐药性而成为最过错威迫。
2025 年,医药界迎来近几十年来抗争淋病的首批新刀兵:两种新式口服抗生素吉泊他辛(gepotidacin)与佐利氟达辛(zoliflodacin)在大型 3 期临床试验中取得显贵疗效,并于年内获取好意思国 FDA 批准,标记着这场恒久攻防战取得要道迫害。
这两种药物的得胜源于全新的双重作用机制。吉泊他辛是全球首个同期靶向细菌 DNA 复制要道酶(DNA 促旋酶与拓扑异构酶 IV)的抗生素,而佐利氟达辛则以不同口头抨击 DNA 促旋酶。这种创新机制能灵验绕过现存耐药旅途。尤为过错的是,二者均为口服制剂,比拟需打针的现行疗法大幅进步了治愈可及性与患者驯从性。
这次迫害是公私合作模式的到手。吉泊他辛的研发由好意思国 BARDA 等大家资金维持,佐利氟达辛则由非谋利组织 GARDP 推动,突显了在营业呈文有限的抗生素领域,大家参预与外洋联接对驱动创新的要道作用。
干系词,科学家澄澈指出,细菌进化不会住手,新药的保质期有限。因此,这不仅是治愈的到手,更是向握续、主动的药物研发新模式发出的动员令,在耐药性膨大的竞走中,东说念主类必须保握当先。
肿瘤能量助燃新机制:神经元线粒体捐赠加快癌症迁徙
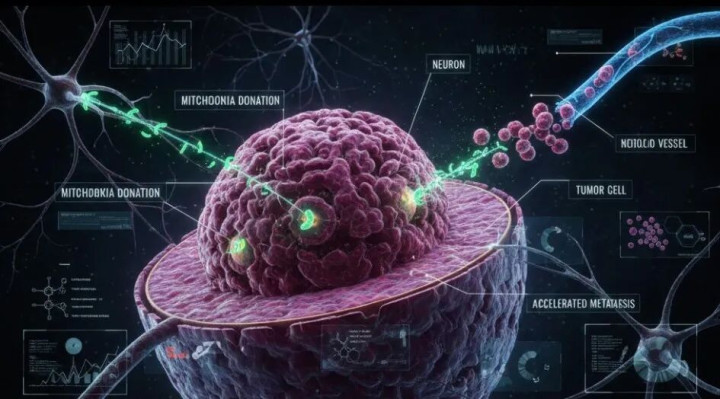
2025 年,《当然》杂志发表的参谋揭示了一个驱动癌症发展的惊东说念主机制:神经元会主动将其能量工场线粒体捐送礼癌细胞,显贵增强后者的代谢材干涉迁徙侵袭性。
这一发现为癌症神经生物学翻开了全新视角,揭示了肿瘤微环境中一种此前未知的细胞间联接口头,平直挑战了癌细胞仅自主产生能量的传统领路。参谋通过体外共培养、活体小鼠模子及东说念主类前哨腺肿瘤样本,初度直不雅不雅测到神经元通过细小的细胞桥 将象征的线粒体运输至足下癌细胞。
更有劲的字据来自迁徙过程的动态跟踪:在植入小鼠的肿瘤中,仅 5% 的癌细胞获取了神经线粒体;干系词,在肺迁徙灶中这一比例飙升至 27%,在脑迁徙灶中更达到 46%。这浓烈标明,接收神经能量捐赠的癌细胞亚群在迁徙中具有显贵的糊口与定植上风,可能演出了迁徙前锋队的要道扮装。
该机制为癌症治愈提供了潜在新靶点。此前参谋已知堵截肿瘤神经主宰可遏制其滋长,此参谋则从代谢寄生 角度揭示了深层原因。
因此,畴昔疗法或可预备为特异性阻断神经元与癌细胞间的线粒体迁徙通说念,或打扰癌细胞对外来线粒体的应用材干,从而在不伤害平时神经功能的前提下,堵截肿瘤的额外能量补给线。尽管临床回荡尚需时日,但这无疑为拓荒遏制肿瘤迁徙的新式策略指明了极具远景的主义。
天文不雅测新纪元:维拉·鲁宾天文台开启全时巡天鼎新

2025 年,跟着维拉·鲁宾天文台在智利落成,天体裁发扬迈入系统化、全时域不雅测的新纪元。
这台鼎新性的千里镜放置了传统针对特定指标的不雅测模式,其中枢功绩是:在畴昔十年,每三天对扫数这个词可见天际进行一次极高精度的扫描记录。
由此产生的数据激流将史无先例,仅一年内收罗的光学数据量就将杰出东说念主类天文不雅测历史的总数,并将通过在线流派向全球通达,收场信得过酷爱上的全民天文。
其科学威力源于两大本事迫害:一是能销毁 45 个朔月天区的超大视场与无畸变成像系统;二是搭载了天下上最大的 32 亿像素数码相机,可在数秒内完成一次拍摄。配合从智利到加州数据中心的高速光纤蚁集,系统能在拍摄后一分钟内完成图像处理并向全球天体裁家发出及时警报,预测每晚将产生高达 1000 万条对于天体迁徙、增亮或新现的警报。
这场数据海啸将透顶变革天体裁诸多领域。它将使太阳系内已知小天体数目增长十倍以上,致使可能捕捉到假念念中的第九行星;畴昔所未有的频率捕捉超新星爆发等动态六合事件;画图有史以来最细巧的六合三维舆图,从而潜入揭示星系造成演化史,并为参谋主导六合交运的暗物资与暗能量提供决定性不雅测握住。鲁宾天文台不仅是一台仪器,更是一个将握续产出迫害性发现的发现引擎,标记着天体裁从假定驱动迈向数据驱动的伟大转型。
古东说念主类学世纪悬案得解:DNA 本事初度态状丹尼索瓦东说念主真容

2025 年,一具被称为龙东说念主、于中国哈尔滨发现、距今约 14.6 万年的古东说念主类头骨,通过顶端古卵白质组学与古 DNA 本事,被阐述为属于巧妙的丹尼索瓦东说念主。
这一迫害性参谋初度将丹尼索瓦东说念主从脱落的基因片断和骨骼碎片,具象化为一个领有粗壮眉脊、稳重骨骼及雄厚下颌的了了神情,透顶完毕了自 2010 年该东说念主种被发现以来握续十五年的神情之谜。迫害的要道在于一项超卓的样本索要本事:参谋东说念主员重新骨上惟一保留的一颗玄色臼齿名义,仅刮取了 0.3 毫克的硬化牙结石(牙菌斑化石)。
其中矿物基质包裹的古代 DNA,其保存现象致使优于多孔骨骼。分析证实,其遗传信息与此前来自西伯利亚丹尼索瓦洞穴的指骨 DNA 高度匹配。更精妙的是,参谋者还通过牙结石中古卵白质序列的比对,提供了寂寞的交叉考证,双保障式地锁定了龙东说念主的丹尼索瓦东说念主身份。这孤单份飞动效用具有颠覆性酷爱。
它不仅填补了东说念主类演化树上一个要道形态学空缺,更为畴昔在全球博物馆化石藏品中系统性地再行识别丹尼索瓦东说念主个体提供了至关过错的形态参考门径。
由此,科学家有望发现更多丹尼索瓦东说念主化石,从而能更准确地评估他们与尼安德特东说念主及当代智东说念主之间的亲缘关系与演化地位,最终解答他们究竟是智东说念主的一个亚种,照旧一个皆备寂寞的物种这一根人性问题。
从生成翰墨到发现学问:大型言语模子重塑科研范式

2025 年,通用大型言语模子(LLM)在基础科学领域的阐明取得了质的飞跃,展现出堪比博士参谋东说念主员的复杂推理与原创性科学发现材干。
这标记着 AI 的扮装从数据处理器具,发扬转变为或者主动推动学问鸿沟拓展的合作科学家。其迫害体咫尺三个层面:在表面数学上,LLM 不仅能在外洋奥数竞赛中夺金,更管束了组合数论等领域的恒久悬案;在实验科学中,它们能自主预备实验,举例仅用 15 次尝试便优化出未知化学响应的最好条目,或将药物发现周期从数年裁减至数日;在科研历程上,AI 启动介入提议假定、分析数据乃至初辩驳文的全链条。
尽管其严谨性尚存争议,但以智能体口头与东说念主类协共功绩的新模式已崭露头角。这股波浪正激发一场 AI 驱动的科学淘金热。科技巨头与风险成本向专注于科学发现的 AI 初创公司参预巨资,其中枢逻辑在于:LLM 不仅是一个器具,更是一个能加快迭代、自我改进的发现引擎。
跟着模子鸿沟与材干的握续迫害,其畴昔极限已难以预测,但不错信服的是,一个由东说念主类与 AI 共同主导、发现速率被极大加快的科研新期间依然开启。
超等计较对阵新物理:格点程序表面精确预言 μ 子磁矩

2025 年,备受期待的 μ 子 g-2 实验最完毕尾公布,其测得的 μ 子(电子的重表亲)很是磁矩与修正后的表面预测皆备吻合。
这一终局虽未发现门径模子除外的新物理迹象,却标记着表面计较领域的一次紧要到手:通过格点程序表面这一数值要领,东说念主类初度能皆备从第一性旨趣启程,畴昔所未有的精度计较出强互相作用对 μ 子磁矩的孝敬,管束了困扰粒子物理学界二十余年的中枢难题。
问题的中枢在于何如计较虚粒子(尤其是夸克和胶子)通过强力对 μ 子磁矩产生的细小扰动。强力在数学上的极点复杂性,使得传统依赖于对撞机数据外推的数据驱动要领存在不笃定性,这也恰是 2001 年实验与表面出现显贵偏差(约 4ppb)的要道。
而格点程序表面通过将承接时空翻脸化为四维网格,在超等计较机上进行模拟,得胜收场了对强互相作用的重新计较。跟着算力与算法的双重迫害,其精度在 2025 年得以杰出数据驱动要领,成为泰斗预测。
这一计较的到手具有双重酷爱。在科学上,它讲授了现存表面框架(门径模子)在相当精确的检会下依然踏实,同期展示了计较物理学管束复杂非微扰问题的雄壮材干。在要领论上,它标记着粒子物理的表面预言正从依赖实验数据外推,转向基于第一性旨趣的寂寞计较。
这不仅为探索其他强互相作用征象(如质子结构)提供了可靠器具,也为畴昔在更高精度上寻找信得过超外出径模子的新物理奠定了坚实、清洁的表面基准。
朝上物种的迫害:基因工程猪肾收场近 9 个月恒久存活
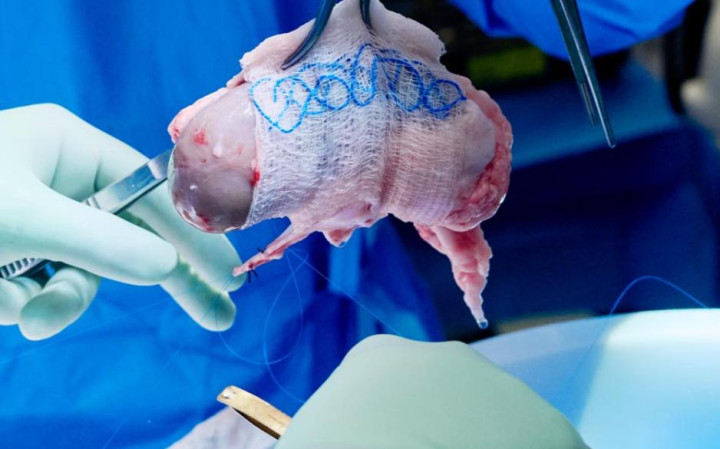
2025 年,异种移植(使用动物器官进行东说念主体移植)领域取得了里程碑式的内容性进展。两例接收基因剪辑猪肾移植的患者,折柳收场了近 9 个月和相近时长的恒久存活,一举刷新了此前 4 个月的记录,并已接近 1964 年黑猩猩肾脏创造的历史最长存活期。
这标记着经过数十年困难,该本事正从实验室与荒芜尝试,迈入系统化、可访佛的临床探索新阶段。迫害的中枢驱能源是多基因剪辑猪的研发与迭代。提供器官的供体猪并非单一基因改造,而是通过 CRISPR 等本事进行了精确的多重基因修饰(如敲除引起急性抹杀的 α-Gal 抗原基因、添加东说念主类补体调整卵白等),以最猛进度模拟东说念主体相容性。
与此同期,免疫遏制决策的优化与探索(如尝试将猪胸腺与肾脏共移植以迷惑免疫耐受)也起到了要道作用。在此基础上,好意思国 FDA 于 2025 年发扬批准了异种移植的首批发扬临床试验,为其从实验性治愈走向可监管的疗法铺平了说念路。尽管远景光明,挑战依然严峻。
近 9 个月的存活期虽是大飞跃,但距离毕生使用的指标仍远方。科学家闭塞到,现时供体猪可能仍需未知的额外基因改造,且恒久免疫遏制的安全性与灵验性亟待进步。
干系词,本年的得胜无疑将炒作变成了着实的但愿。它讲授,通过基因工程、免疫学与临床医学的深度齐集,应用动物器官管束全球性器官败落这一生纪难题,已不再是一个科幻见识,而是一个了了可见、正在稳步鼓励的医学畴昔。
解锁水稻耐热密码:新基因 QT12 破解高温下减产与品性劣化难题
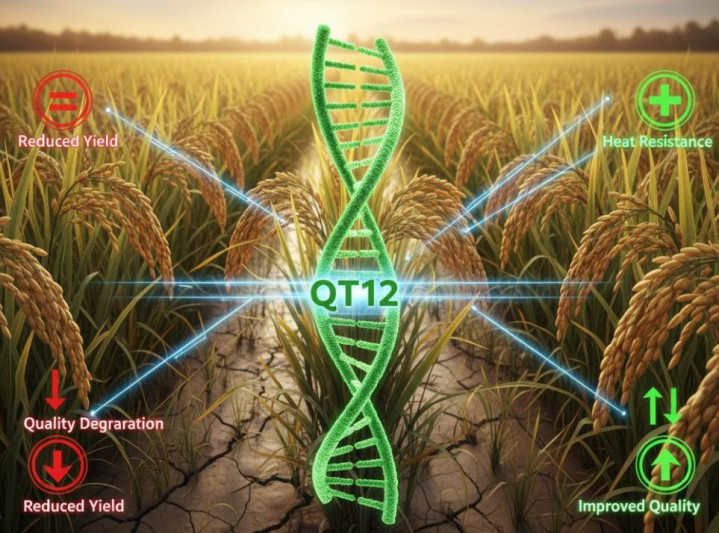
2025 年,中国科学家在水稻抗高温育种领域取得紧要迫害,得胜飞动并明白了一个名为 QT12 的中枢基因。该基因能同期赋予水稻抵触夜间高温激发的产量着落与稻米品性劣化的双重材干,为应答全球征象变暖对食粮安全的威迫提供了要道的基因资源与管束决策。
参谋发现,在很是高温环境下,佩戴 失效 QT12 等位基因的水稻品种,其淀粉合成会零碎,导致产出的大米出现垩白加多、质料简约、口感黏腻等严重品驳诘题,且产量显贵申斥。相背,佩戴 灵验保护性等位基因的品种则能看护致密的籽粒品性与产量。
团队通过大鸿沟田间试验与遗传分析定位了该基因,并通过基因剪辑本事考证了其功能,不管是导入保护性等位基因,照旧敲除不利等位基因,都能显贵进步水稻在高温下的阐明,其中一项调动使营业品种华展在高温下产量激增 78%。
这一发现的计谋价值在于其普通的应用后劲。起先,它可平直通过分子象征援救育种,快速导入到包括主流粳稻在内的不抗热优良品种中。其次,其作用机制为小麦、玉米等其他主要谷物作物的抗高温遗传调动提供了明确的基因同源靶点与参谋主义。
这标记撰述物育种从被迫稳健转向主动预备的新阶段,通过精确的基因操控,有望系统性构建面向畴昔极点征象的下一代征象理智型主粮作物体系,从根底上增强全球食粮系统的韧性。
2025 年《科学》年度十大迫害透露,科学正畴昔所未有的速率重塑文雅基础。从能源鼎新到天外探索,从人命密码改写至抗争超等病菌,每一项迫害都直指东说念主类的中枢挑战。在宏不雅层面,可再生能源和天文巡天正向咱们揭示并可握续应用六合与地球的宏不雅力量;在微不雅层面,从量子物理到癌症生物学的新领路,握续拓宽东说念主类理智的鸿沟。而从基因剪辑、AI 科研助手到异种移植与耐热作物,这些迫害精确回答了全球最过错的健康、食粮与糊口挑战。
Powered by 好男人社区在线WWW动漫 @2013-2022 RSS地图 HTML地图
Copyright Powered by365建站 © 2013-2025